¿Qué es la reacción endotérmica? ¿Qué es la reacción exotérmica? ¿Cómo ocurren? ¿Cuáles son las diferencias entre las reacciones endotérmicas y exotérmicas?
Diferencias entre las Reacciones Endotérmicas y Exotérmicas
La diferencia entre las reacciones endotérmicas y exotérmicas radica en las propias palabras. «Térmico» se refiere al calor, al igual que en la palabra «termómetro». «Exo» significa «afuera» y «endo» significa «adentro». Por lo tanto, una reacción endotérmica atrae el calor hacia un objeto o área, mientras que una reacción exotérmica expulsa calor. A partir de esta definición básica de los términos, puede comprender una variedad de otros datos sobre estos dos tipos de reacción química.
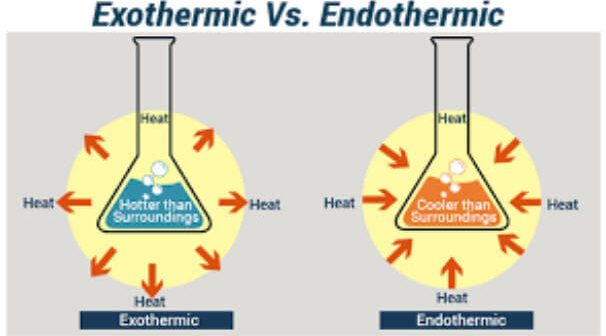
Reacciones endotérmicas enfrían sus alrededores
Desde el punto de vista de la química, no existe el frío, solo la ausencia de calor. Las reacciones endotérmicas atraen energía calorífica a sí mismas. A medida que el calor abandona el área circundante, la temperatura desciende. Por ejemplo, una compresa fría de primeros auxilios químicos funciona debido a una reacción endotérmica entre el agua y el nitrato de amonio. Debido a que atrae la energía térmica hacia el paquete, el paquete se siente frío al tocarlo, ya que extrae calor del área circundante.
Las reacciones endotérmicas contienen más energía
Las reacciones endotérmicas atraen y almacenan energía en forma de enlaces químicos producidos por la reacción. En una reacción endotérmica, el producto contiene más energía neta que los reactivos al inicio del proceso. Los productos de las reacciones endotérmicas generalmente tienen más volumen debido a la energía almacenada.
Las reacciones exotérmicas hacen que el ambiente sea más cálido
Una reacción exotérmica arroja energía térmica a medida que avanza la reacción, lo que significa que irradia calor mientras se está produciendo. En una fogata, la energía de los enlaces químicos de la madera y el papel se libera en forma de calor y luz. Esa energía liberada calienta el área circundante para los campistas fríos.
Las reacciones exotérmicas contienen menos energía
En cualquier reacción exotérmica, la energía se elimina de los enlaces químicos en los reactivos. Por lo general, esto requiere un bit de energía inicial llamado «energía de activación» para iniciar el proceso, como una cerilla encendida u otra aplicación de calor para iniciar esa fogata. Una vez finalizado el proceso exotérmico, el producto tiene menos calor y generalmente es más compacto.


