Si bien estos dos números comparten elementos comunes, revelan información bastante diferente sobre los átomos.
Cada uno de estos números son medidas de características específicas de los átomos. Debido a las leyes que dictan los átomos y las partículas que los componen, a menudo se puede suponer correctamente que si uno está más alto en un átomo en particular, el otro también estará más alto en ese átomo. Pueden aplicarse algunas excepciones.

Fuente : pixabay.com
Masa atomica
La masa atómica se mide en unidades de masa atómica a menudo indicadas por la abreviatura «amu». Una unidad de masa atómica es igual a 1/12 de la masa de un átomo de carbono-12. Decir que en gramos, una uma es igual a aproximadamente 1,66 × 10-24 gramos. Estos son números bastante pequeños en relación con la mayoría de las mediciones que se realizan en la vida diaria, pero los científicos han desarrollado formas de medir estas cantidades con una precisión constante. La espectrografía de masas es uno de los métodos más comunes utilizados para medir la masa atómica de un átomo.
Gran parte de la masa de un átomo se encuentra en el núcleo del átomo y está en forma de protones y neutrones. Cada una de estas partículas pesa aproximadamente una unidad de masa atómica. El número de masa es el recuento de estas partículas, por lo que el número de masa está muy cerca de la masa atómica.
Número atómico
El número atómico se refiere al número de protones en el núcleo. A menudo se denota con el símbolo Z. El número de electrones en el átomo neutro es igual al número de protones en el núcleo y, por lo tanto, es igual al número atómico del átomo.
Los números atómicos fueron asignados por primera vez alrededor de 1913 por H. G. J. Moseley. Organizó los átomos en un orden basado en la observación de espectros de rayos X y luego los numeró. Los elementos están ordenados en la tabla periódica por su número atómico.
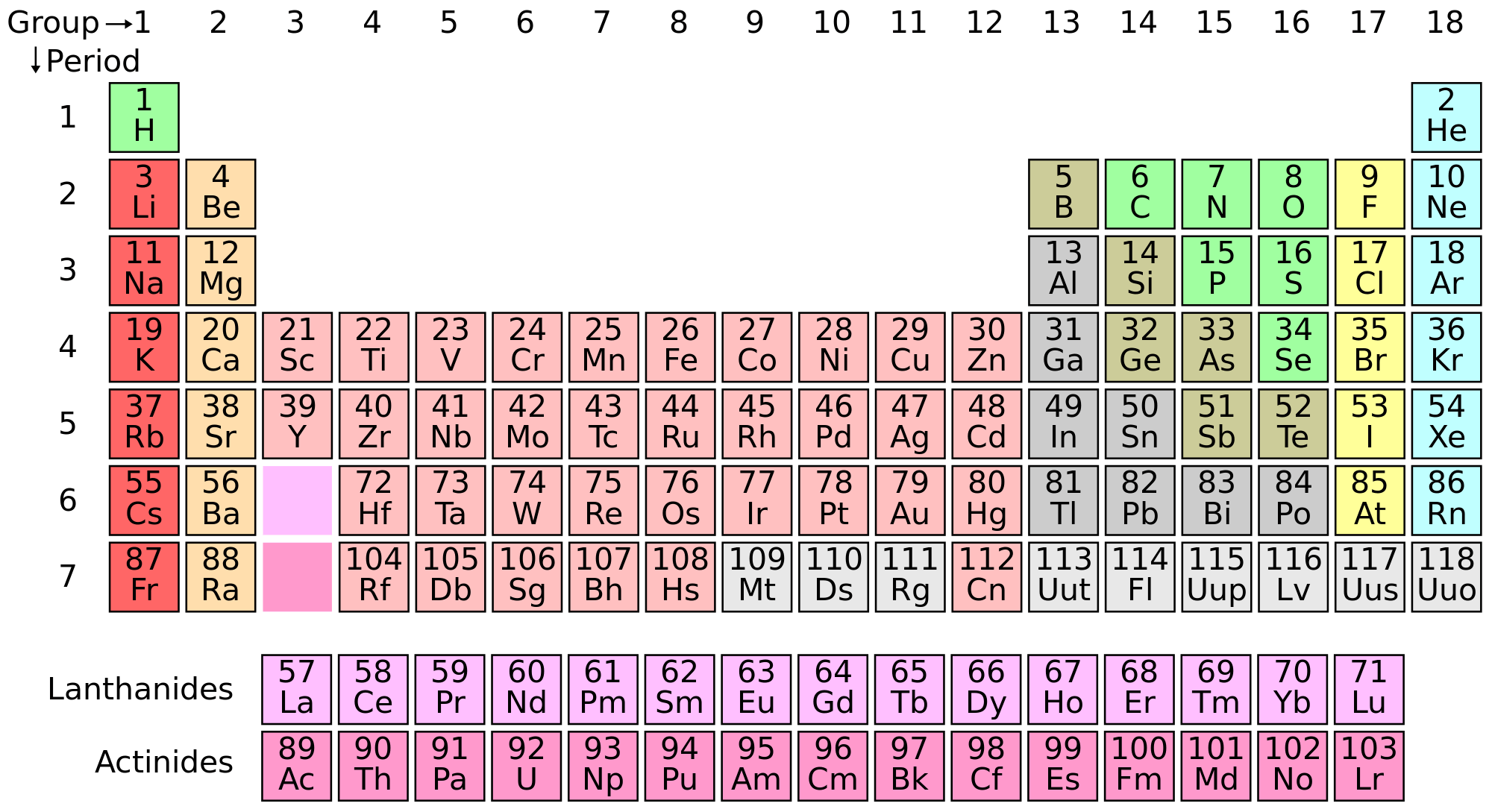
Fuente : pixabay.com
Descripción general
Es posible que ya reconozca cuán estrechamente relacionados están estos dos números. Si el número atómico es alto, se puede esperar que la masa atómica también sea alta. Este es el resultado de que los protones numerados en el número atómico representan una fracción de la masa en el núcleo.
Hay una serie de otros números significativos al examinar los átomos. Estos incluyen el peso atómico que está estrechamente relacionado con la masa atómica y fue la base de la ley periódica de Mendeleev.


