En esta publicación se explica qué es la tensión superficial y se describen las causas que la generan. Además, se proporcionan ejemplos para una mejor comprensión.
Definición de la Tensión Superficial y Causas
Definición de la tensión superficial
La tensión superficial es una propiedad física igual a la cantidad de fuerza por unidad de área necesaria para expandir la superficie de un líquido. Es la tendencia de una superficie fluida a ocupar el área de superficie más pequeña posible. La tensión superficial es un factor principal en la acción capilar. La adición de sustancias llamadas surfactantes puede reducir la tensión superficial de un líquido. Por ejemplo, agregar detergente al agua disminuye su tensión superficial. Mientras que la pimienta rociada sobre el agua flota, la pimienta rociada sobre el agua con detergente se hundirá.

Las fuerzas de tensión superficial se deben a fuerzas intermoleculares entre las moléculas del líquido en los límites externos del líquido.
Las unidades de tensión superficial son energía por unidad de área o fuerza por unidad de longitud.
Ejemplos de tensión superficial
La tensión superficial permite que algunos insectos y otros animales pequeños, que son más densos que el agua, caminen por su superficie sin hundirse.
La forma redondeada de las gotas de agua sobre una superficie se debe a la tensión superficial.
Las lágrimas de vino forman riachuelos en el vaso de una bebida alcohólica (no solo vino) debido a la interacción entre los diferentes valores de tensión superficial del etanol y el agua y la evaporación más rápida del alcohol en comparación con el agua.
El aceite y el agua se separan debido a la tensión entre dos líquidos diferentes. En este caso, el término es «tensión de interfaz», pero es simplemente un tipo de tensión superficial entre dos líquidos.
Cómo funciona la tensión superficial
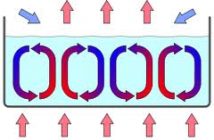
En la interfaz entre un líquido y la atmósfera (generalmente aire), las moléculas líquidas se atraen más entre sí que a las moléculas de aire. En otras palabras, la fuerza de cohesión es mayor que la fuerza de adhesión. Debido a que las dos fuerzas no están en equilibrio, se puede considerar que la superficie está bajo tensión, como si estuviera encerrada por una membrana elástica (de ahí el término «tensión superficial». El efecto neto de cohesión versus adhesión es que existe una Fuerza en la capa superficial. Esto se debe a que la capa superior de moléculas no está rodeada por líquido en todos los lados.
El agua tiene una tensión superficial especialmente alta porque las moléculas de agua se atraen entre sí por su polaridad y pueden participar en enlaces de hidrógeno.